下一代重磅药物?全球首个环状RNA药物获FDA临床试验许可
发布时间:2024-12-13 22:45分类: 无 浏览:140评论:0


▲全球首个环状RNA药物RXRG001获FDA临床试验许可
一类独特的非编码RNA分子
环状RNA简介

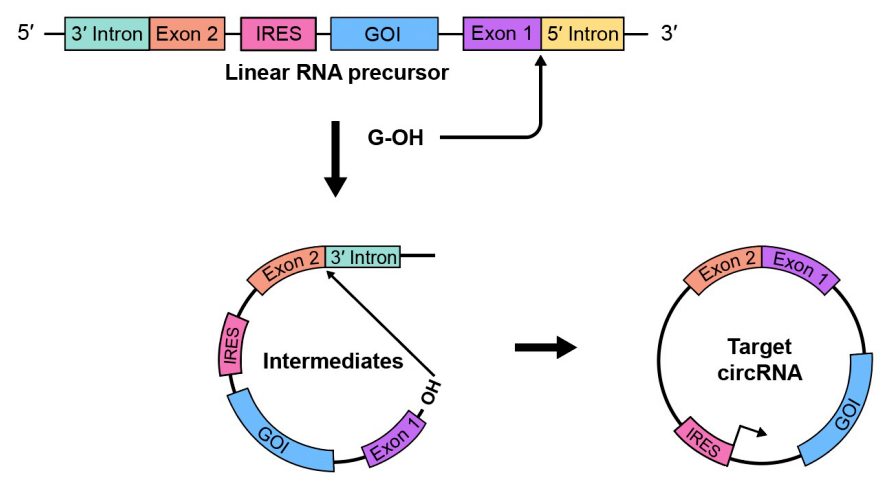
▲环状RNA的生物合成过程与功能
从“RNA剪接副产品”到临床应用
环状RNA的发现与发展
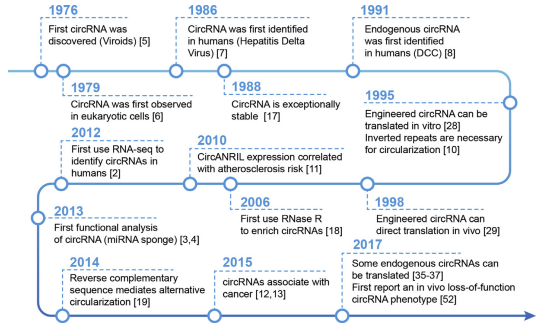
随着对circRNA功能的深入理解,科学家开始探索其在临床治疗中的潜力。因其稳定性、特异性表达和多功能性,circRNA被视为潜在的生物标志物和治疗工具。尤其在癌症领域,研究发现某些circRNA在特定癌症中具有显著的诊断和预后价值。
从基因调控到精准医疗
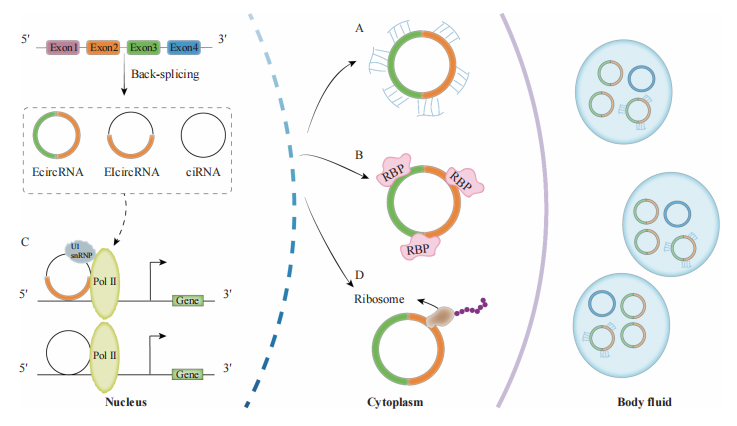
环状RNA的多种生物学功能
尽管环状RNA在细胞中相对稀少,仅占非核糖体RNA的约0.1%,但其独特的共价闭合结构为其带来了多种生物学功能。
1. miRNA的“海绵”作用
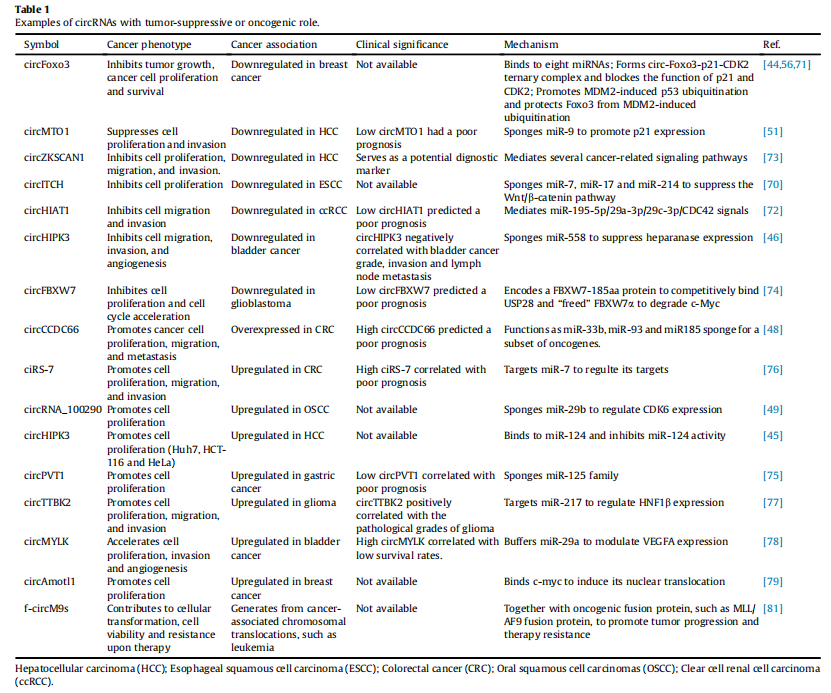
circRNA能够作为miRNA的“海绵”,通过捕捉和隔离特定miRNA,减少其对靶mRNA的抑制。这一机制在癌症等疾病治疗中尤为关键,circRNA可以通过调节miRNA活性,间接影响多种基因的表达。例如,circRNA可吸附与癌症相关的miRNA,从而调控肿瘤细胞的增殖、转移及抗药性,为癌症及病毒感染的治疗提供了新思路。
2. 调节蛋白质功能
虽然多数circRNA被认为是非编码分子,但一些circRNA已被证实能够编码小肽,这些小肽在细胞信号传导和细胞周期调控中发挥重要作用。通过内部核糖体进入位点(IRES),circRNA可启动小肽的翻译,拓展其在代谢调节和抗衰老治疗中的应用潜力。
反义circRNA是一类设计成与特定靶RNA序列互补的分子,可通过与RNA-RNA结合抑制目标RNA的翻译。这种设计在抗病毒治疗中显示出特别的潜力,例如靶向COVID-19病毒基因组的保守区域以抑制病毒增殖。此外,反义circRNA还能引导腺苷脱氨酶(ADARs)实现RNA编辑,拓展其在基因修饰中的应用前景。
5. 免疫调控功能
6. 作为疾病的生物标志物
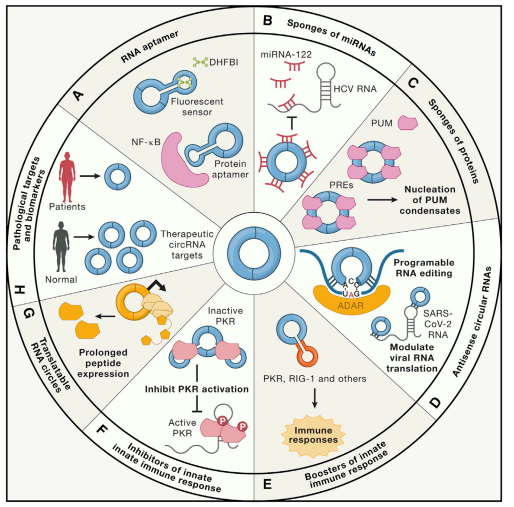
▲ 以环状RNA为基础的生物学应用
潜力巨大,但面临多重挑战
环状RNA的优势与挑战
尽管miRNA、lncRNA和circRNA都在基因表达调控中发挥作用,但circRNA因其环状结构具备独特优势,在临床治疗中展现出更大的潜力。
▶▶ 高度稳定性
▶▶ 靶向特异性表达
▶▶ 多功能性与灵活性
▶▶ 创新的RNA编辑与病毒靶向潜力
▶▶多重挑战与技术突破点
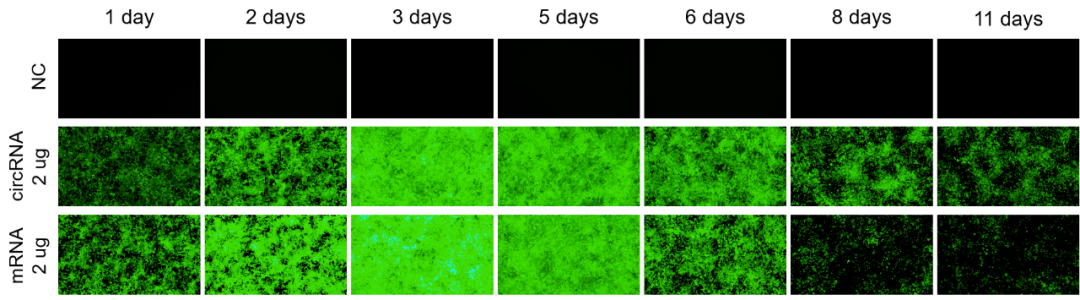
云舟生物IVT circRNA平台
【参考资料】
[1]https://www.prnewswire.com/news-releases/ribox-therapeutics-announces-fda-clearance-for-ind-application-of-rxrg001-the-first-circular-rna-therapy-for-the-treatment-of-radiation-induced-xerostomia-and-hyposalivation-302287539.html
[2]Chen B, Dragomir MP, Yang C, Li Q, Horst D, Calin GA. Targeting non-coding RNAs to overcome cancer therapy resistance. Signal Transduct Target Ther. 2022;7(1):121. Published 2022 Apr 13. doi:10.1038/s41392-022-00975-3
[3]Qu S, Liu Z, Yang X, et al. The emerging functions and roles of circular RNAs in cancer. Cancer Lett. 2018;414:301-309. doi:10.1016/j.canlet.2017.11.022
[4]Ma L, Chu H, Wang M, Zhang Z. Biological functions and potential implications of circular RNAs. J Biomed Res. 2022;37(2):89-99. doi:10.7555/JBR.36.20220095
[5]Liu CX, Chen LL. Circular RNAs: Characterization, cellular roles, and applications. Cell. 2022;185(13):2390. doi:10.1016/j.cell.2022.06.001
VectorBuilder云舟生物(以下简称“云舟生物”)是世界知名分子生物学家蓝田博士创办的基因递送领军企业,在全球设有10余家子公司和办事处,2023年晋升为全球独角兽企业。
云舟生物独创“载体家”平台,开启了个性化基因载体的商品化时代;目前已赋能全球90多个国家和地区,为超过4500家顶尖科研院校和制药公司提供服务,在QS前100高校的客户覆盖率达到了90%,全球TOP30药企的客户覆盖率亦超过90%,产品成果的全球文献引用量逾5000篇。
云舟生物的基因药物CRO、CDMO项目遍布北美、欧洲、日本等多个国家和地区,已成功助力全球数十个项目成功开展IIT或IND研究,其中GMP级别的质粒和慢病毒载体已获得美国FDA的IND正式批准,用于在美国的多中心临床试验。
云舟生物致力于系统性攻克基因递送行业的关键技术瓶颈,为行业和世界创造不可取代的价值。






- 排行
-
- 1携手华为,共创金融新纪元 —— 赢时胜亮相2024华为全联接大会,共绘金融科技生态蓝图
- 2朗新集团、蚂蚁链完成首单新能源RWA,助储充产业提“智”增效
- 3理论深度分析Autosar CAN 时间同步
- 4万字长文,建议收藏——当要求功能安全时,我们在要求什么?
- 5最新解读 | 2024年山东卷高考生物试题浅析
- 62024年河南商丘市虞城县教育人才服务中心人才引进15人公告
- 7China-Serbia Youth International Cultural Exchange Program Ends!
- 8满心热爱,奔赴星辰!英华2024-2025学年开学典礼圆满举行
- 9聚焦三大核心能力培养,这家企业是怎么做好新员工培训的?
